Ecoulements permanents
Exercice 69 ⭐️ Diagrammes de Mollier, Spé/L2
Tracer l’allure d’un diagramme de Mollier () pour un fluide et indiquer les phases en présence.
Quelle est l’allure des isenthalpiques ?
Quelle est l’allure des isothermes si le gaz se comporte comme un gaz parfait ?
Comment lire sur le diagramme la valeur des enthalpies massiques de vaporisation ?
Montrer que, dans le diagramme de Mollier, la pente des courbes isentropiques est positive.
Montrer que, sur une courbe isenthalpique du diagramme de Mollier, l’entropie est une fonction décroissante de la pression.
Corrigé
Allure d’un diagramme de Mollier
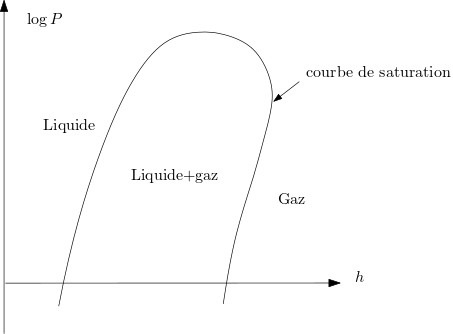
Les isenthalpiques sont par définition des droites verticales.
Pour un gaz parfait, une isotherme est une isenthalpique, donc une portion verticale sur le diagramme du côté gaz.
Dans la région (liquide + gaz), une isotherme est une isobare, donc un segment horizontal.
Pour une phase condensée (indilatable incompressible en première approximation), l’enthalpie ne dépend que de la température, une isotherme est à nouveau une portion de droite verticale.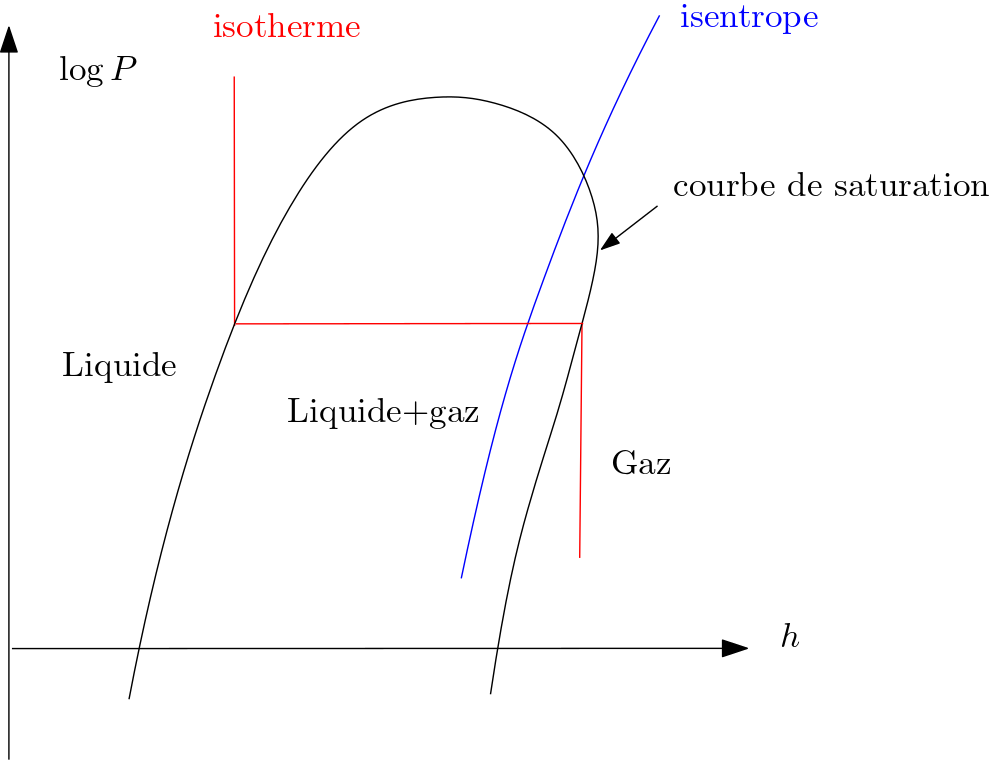
L’enthalpie massique de vaporisation à est la longueur du segment horizontal à l’intérieur de la courbe de saturation à la pression de vapeur saturante .
. Cette expression, valable dans le cas d’une phase, l’est aussi dans le cas d’un système diphasé, dont la composition varie (voir Remarque à la fin).
Pour une isentropique . Comme est une fonction croissante ., l’entropie est bien une fonction décroissante de , et donc de .
Remarque — Avec les enthalpies massiques du liquide saturant et de la vapeur saturante, les entropies massiques du liquide saturant et de la vapeur saturante,
d’où
Avec ,
Exercice 147 ⭐️ Ecoulement d’un gaz dans une conduite, Spé/Classique
Du diazote assimilé à un gaz parfait diatomique s’écoule dans une conduite horizontale, rigide et calorifugée. La vitesse d’entrée du gaz est 300 m.s et la vitesse de sortie 500 m.s Les pressions d’entrée et de sortie sont respectivement bars et bar. La masse molaire est g.
Quelle est la variation de température du gaz?
Calculer la variation d’entropie de l’unité de masse du gaz, l’entropie créée et l’entropie échangée. La température d’entrée est 300 K.
Corrigé
- Le premier principe appliqué aux écoulements permanents s’écrit
avec les notations usuelles : énergie cinétique, énergie potentielle et enthalpie massiques, transfert thermique massique et travail utile massique reçu (hors celui des forces de pression en amont et en aval).
La conduite est horizontale, l’énergie potentielle de pesanteur ne varie pas.
Les parois de la conduite sont calorifugées, donc .
Les parois de la conduite sont rigides, donc .
En désignant par la vitesse, .
Pour un gaz parfait diatomique
.
D’où
A.N.
- L’identité thermodynamique s’écrit pour les grandeurs massiques
d’où pour le gaz parfait ()
, soit
L’entropie échangée puisqu’il n’y a pas de transfert
thermique. La relation
donne
Exercice 148 ⭐️⭐️⭐️ Turboréacteur, Centrale PC, Spé
Dans un turboréacteur utilisé pour les avions, la propulsion provient
de la combustion du kérosène dans le dioxygène de l’air.
Une part de l’énergie produite est récupérée par une turbine qui sert à faire tourner un compresseur. On fait les hypothèses suivantes :
-De (1) à (2) et de (3) à (5) , le fluide est assimilé à un gaz parfait. Bien que la combustion du kérosène produise de l’eau et du dioxyde de carbone, on considère que la capacité thermique massique à pression constante du gaz dans son ensemble varie peu dans les différentes phases , ainsi que sa constante . Le débit massique de l’air entrant est égal à 50 . Le régime est supposé permanent ;
-On néglige les variations d’énergie potentielle, les pertes dues aux frottements et les variations d’énergie cinétique (sauf en sortie des tuyères) ;
-la puissance mécanique nécessaire au fonctionnement du compresseur est fournie par la turbine ;
-les évolutions dans le compresseur, la turbine et la
tuyère sont supposées adiabatiques réversibles. La combustion est
isobare. Le pouvoir calorifique du kérosène vaut .
Les différentes étapes suivies par le gaz dans le turboréacteur sont les suivantes
(1) à (2) : l’air, à la température et à la pression , est comprimé avec un taux de compression ;
(2) à (3) : la combustion est isobare et à la sortie, le gaz a la température ;
(3) à (4) : le gaz subit une détente dans la turbine jusqu’à la pression ;
(4) à (5) : le gaz se détend dans la tuyère jusqu’à la pression ambiante et la température .
Préciser les valeurs manquantes des pressions et températures .
Calculer le débit de kérosène nécessaire.
Définir, exprimer et calculer le rendement du turboréacteur.
Réflexes
- Gaz parfait en évolution adiabatique réversible 👉 La loi de Laplace s’applique.
- Réaction de combustion du kérosène 👉 Une réaction de combustion est rapide, faire un bilan enthalpique comme quand on calcule une température de flamme en thermochimie.
- Écoulement en régime permanent 👉 Premier principe “industriel” pour les écoulements permanents.
Corrigé
Les évolutions dans le compresseur sont isentropiques. Le gaz étant considéré parfait, la loi de Laplace s’applique. En variables
On en déduit .
A.N. et .
De même
A.N.À partir de la combustion d’une masse de kérosène dans d’air, on obtient une masse de gaz mélange de . Le bilan enthalpique s’écrit pour la réaction de combustion rapide, donc adiabatique , d’où
A.N. .Le rôle du turboréacteur est d’éjecter des gaz à grande vitesse, on cherche à avoir une grande énergie cinétique des gaz éjectés.
Comme la puissance mécanique nécessaire au fonctionnement du compresseur
est fournie par la turbine, la seule grandeur coûtante est le kérosène.
Le rendement est défini par
où est l’énergie cinétique massique des gaz éjectés.
Pour obtenir , on applique le premier principe appliqué aux
écoulements permanents entre (4) et (5) :
car l’écoulement dans
la tuyère est adiabatique et sans travail utile (les parois de la
tuyère sont indéformables).
et l’énergie cinétique en (4) est négligeable. D’où , soit
et
A.N. .
Ce rendement est bien sûr surestimé car on a fait des hypothèse simplificatrices de fonctionnement idéal.